El folículo piloso humano no comienza como una simple estructura destinada a producir cabello. Desde su origen, se comporta como un mini-órgano altamente especializado, cuya formación depende de una secuencia precisa de eventos embriológicos, interacción epitelio-mesenquimal y redes de señalización molecular finamente reguladas.
Comprender su desarrollo embriofetal no solo enriquece la embriología cutánea, sino que también aporta fundamentos esenciales para la tricología moderna, la dermatología regenerativa y la comprensión profunda de la biología capilar.
El origen: la piel como escenario biológico
El desarrollo del folículo piloso ocurre dentro de la embriología de la piel. La epidermis deriva del ectodermo superficial, mientras que la dermis proviene principalmente del mesénquima de origen mesodérmico; en regiones cefálicas, además, existe contribución de la cresta neural a componentes específicos, como melanocitos y parte del tejido conectivo craneofacial. Este contexto es crucial, porque el folículo no se forma de manera aislada: emerge dentro de una piel fetal en construcción, en un microambiente biológicamente competente para inducir anexos cutáneos.
Durante las primeras semanas de gestación, antes de que exista un folículo reconocible, se organiza la epidermis primitiva, aparece el peridermo transitorio, se especializa progresivamente el mesénquima dérmico y se establece la membrana basal.
En esta etapa todavía no hay cabello, pero sí existe una preparación tisular indispensable para que posteriormente se active el programa folicular.
La interacción epitelio-mesenquimal: el principio organizador
La embriogénesis del folículo piloso es uno de los modelos clásicos de interacción epitelio-mesenquimal recíproca.
El mesénquima dérmico emite señales inductivas sobre regiones específicas de la epidermis; esta, a su vez, responde, modifica su destino biológico y retroalimenta al mesénquima. De esa conversación surgen la inducción folicular, la invaginación epitelial, la organización de la condensación dérmica y la formación progresiva de las estructuras profundas del folículo.
En otras palabras, el folículo piloso no nace como una “prolongación” de la piel, sino como el resultado de un diálogo molecular y morfogenético altamente coordinado. Esa visión es hoy central para entender por qué el folículo tiene capacidad regenerativa, por qué responde a señales locales y sistémicas, y por qué su biología va mucho más allá del tallo piloso visible.
De la placoda al folículo fetal completo
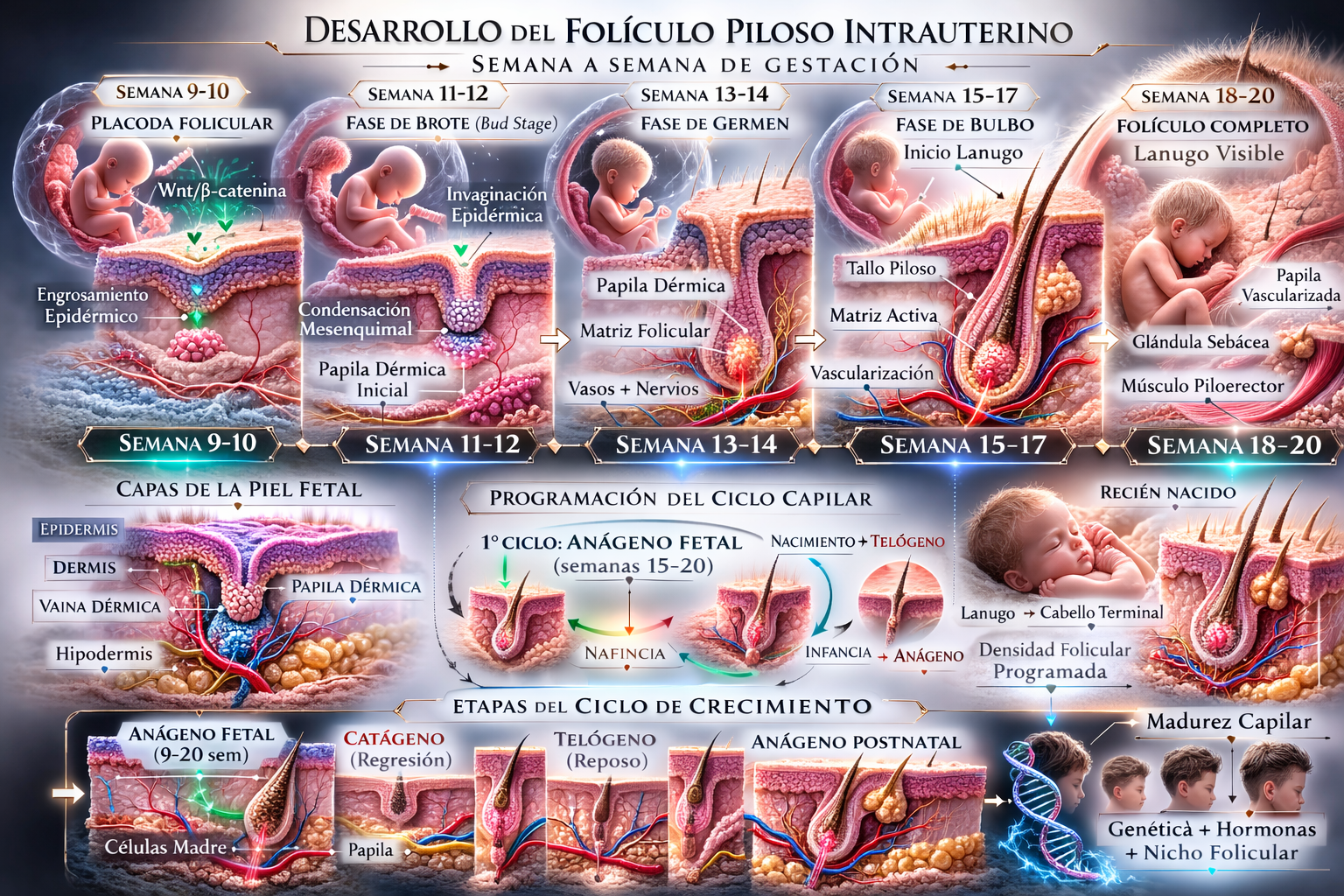
La primera evidencia morfológica del desarrollo folicular aparece alrededor de las semanas 9 a 10 de gestación con la formación de la placoda folicular, un engrosamiento focal de la epidermis que marca el inicio visible del destino anexial.
Esta fase depende de manera crítica de la vía Wnt/β-catenina, considerada un disparador mayor de la morfogénesis folicular.
Posteriormente, entre las semanas 11 y 12, el epitelio placodal se invagina hacia la dermis formando el brote folicular. Más adelante, entre las semanas 13 y 14, emerge el germen piloso, etapa en la que la estructura gana complejidad tridimensional y profundiza su relación con la condensación dérmica. Entre las semanas 15 y 17 se organiza el bulbo piloso, y entre las 18 y 20 semanas el folículo adquiere una arquitectura fetal mucho más madura, con papila dérmica, matriz, vainas radiculares y pelo fetal en desarrollo.
Señalización molecular: la gramática del desarrollo folicular
La formación del folículo piloso está gobernada por vías de señalización conservadas y altamente integradas. Wnt/β-catenina es esencial para la inducción placodal; Sonic Hedgehog favorece el crecimiento profundo y la expansión del germen; BMP regula patrón, densidad y equilibrio proliferativo; Notch participa en la diferenciación celular; y EDA/EDAR/NF-κB interviene en la organogénesis de los anexos ectodérmicos.
Más que actuar por separado, estas vías funcionan como una red coordinada que define tiempo, posición y destino celular.
Este marco molecular tiene un enorme valor clínico y conceptual. Muchas de las alteraciones que más tarde interpretamos en tricología, ya sea desde la miniaturización, la regeneración o la susceptibilidad folicular, descansan sobre mecanismos que inicialmente fueron establecidos durante la embriogénesis.
Papila dérmica, matriz y nicho folicular
A medida que el folículo madura, se diferencian sus compartimentos funcionales. La papila dérmica surge de la condensación mesenquimal y se convierte en el principal centro regulador del órgano piloso, influyendo sobre proliferación, diferenciación y ciclicidad. La matriz folicular se organiza alrededor de ella y se transforma en la zona proliferativa encargada de generar el tallo piloso y parte de las vainas radiculares.
En paralelo, se establece progresivamente la región del bulge o promontorio, localizada en relación con la inserción del músculo piloerector. Esta zona constituye el nicho de células madre foliculares y representa una de las bases más importantes de la capacidad regenerativa del folículo.
En humanos, el bulge ha sido identificado como un reservorio esencial de células con plasticidad biológica y relevancia clínica.
La glándula sebácea y la unidad pilosebácea
La embriología de la glándula sebácea sigue la del folículo piloso. Su desarrollo comienza aproximadamente entre las semanas 13 y 16 de gestación, originándose como una evaginación lateral del epitelio folicular. Más adelante, sus células se diferencian en sebocitos y contribuyen a la función protectora del tegumento fetal.
Este dato es especialmente importante porque demuestra que el folículo piloso no debe entenderse por separado, sino como parte de la unidad pilosebácea, donde folículo, glándula sebácea y músculo piloerector conforman una organización anatómica y funcional integrada.
El lanugo: primera expresión funcional del folículo fetal
Uno de los hitos más relevantes del desarrollo fetal es la producción de lanugo, un pelo fino, suave y no terminal que suele comenzar a hacerse visible entre las semanas 16 y 20, y que se distribuye de manera más amplia en el segundo trimestre.
El lanugo cumple funciones protectoras dentro del ambiente intrauterino, favorece la adhesión del vernix caseoso y refleja que el folículo fetal ya ha alcanzado un nivel funcional significativo.
Su presencia no debe interpretarse como una etapa “inmadura” en sentido peyorativo. Por el contrario, el folículo fetal es altamente activo, pero trabaja en un entorno protegido. Produce, crece y se organiza antes del nacimiento, aunque todavía no está sometido al estrés ambiental, a la microbiota postnatal ni a la carga adaptativa propia del ciclo piloso adulto. Esta es una de las ideas más finas y elegantes de la embriología capilar.
¿Existe ciclo piloso antes de nacer?
En la vida fetal no encontramos un ciclo piloso completo como el del adulto. Más bien existe una dinámica que puede describirse como un ciclo piloso rudimentario: predominio de anágeno prolongado, producción sostenida de lanugo y ausencia de un telógeno verdadero intrauterino.
La primera fase telógena real aparece después del nacimiento, en el contexto postnatal temprano.
El folículo fetal no “descansa” como el adulto, porque no se encuentra todavía expuesto a un entorno desafiante. Su dinámica está adaptada a la vida intrauterina, y solo tras el nacimiento comienza la transición hacia un ciclo más complejo, influenciado por hormonas, microbiota, oxigenación ambiental e interacción inmunológica más amplia.
Del nacimiento a la biología capilar visible
Al nacer, el folículo ya ha establecido una arquitectura básica, un nicho regenerativo, una papila funcional, una matriz activa y una integración pilosebácea organizada. En otras palabras, el órgano capilar no comienza con la infancia: llega al nacimiento con una memoria biológica ya trazada. La transición posterior no consiste en “crear” el folículo, sino en exponer un órgano ya formado a un nuevo mundo biológico.
Una mirada clínica y científica
Entender la embriología del folículo piloso no es un lujo académico. Es una base imprescindible para interpretar mejor la biología del cuero cabelludo, la fisiopatología de las alopecias, la respuesta folicular a los tratamientos y el futuro de la medicina regenerativa capilar. Cada etapa del desarrollo embriofetal deja una huella en la organización del órgano piloso adulto.
En Clínica Capilar, creemos que la verdadera medicina capilar comienza donde otros solo ven cabello: en la ciencia del folículo piloso, en su anatomía, en su fisiología y en su historia biológica desde antes del nacimiento. Ese enfoque permite una valoración más profunda, más personalizada y más rigurosa de cada paciente. Porque tratar el cabello con excelencia exige comprender primero el órgano que le da origen.
Bibliografía
- Park S, Lee J, Choi JW. Hair Follicle Morphogenesis During Embryogenesis, Neogenesis, and Regeneration. Int J Mol Sci. 2022;23(12):6874.
- Millar SE. Molecular mechanisms regulating hair follicle development. J Invest Dermatol. 2002;118(2):216-25.
- Andl T, Reddy ST, Gaddapara T, Millar SE. Wnt signals are required for the initiation of hair follicle development. Dev Cell. 2002;2(5):643-53.
- Shamloul G, Khachemoune A. An updated review of the sebaceous gland and its role in health and diseases. Part 1: Embryology, evolution, structure, and function of sebaceous glands. Dermatol Ther. 2021;34(1):e14695.
- Saxena N, Mok KW, Rendl M. An updated classification of hair follicle morphogenesis. Exp Dermatol. 2019;28(3):332-44.
- Müller M, Jasmin JR. Embryology of the hair follicle. Early Hum Dev. 1991;26(3):159-66.
- Rishikaysh P, Dev K, Diaz D, Qureshi WM, Filip S, Mokry J. Signaling involved in hair follicle morphogenesis and development. Int J Mol Sci. 2014;15(1):1647-70.
- Lavker RM, Sun TT, Oshima H, Barrandon Y, Akiyama M, Ferraris C, et al. Hair follicle stem cells. J Invest Dermatol Symp Proc. 2003;8(1):28-38.
- Ohyama M, Terunuma A, Tock CL, Radonovich MF, Pise-Masison CA, Hopping SB, et al. Characterization and isolation of stem cell-enriched human hair follicle bulge cells. J Clin Invest. 2006;116(1):249-60.
- Verhave BL, Lall N, Muncie HL Jr. Embryology, Lanugo. StatPearls. Treasure Island (FL): StatPearls Publishing; 2022.
- Martel JL, Chan C. Anatomy, Hair Follicle. StatPearls. Treasure Island (FL): StatPearls Publishing; 2024.
- Houschyar KS, Borrelli MR, Tapking C, Popp D, Puladi B, Ooms M, et al. Molecular mechanisms of hair growth and regeneration. Plast Reconstr Surg. 2020;145(3):702e-715e.